Het kandidaat-chikungunya-vaccin VLA1553 werd over het algemeen goed verdragen en veroorzaakte een immuunrespons bij 99% (263/266) van de deelnemers, volgens een fase 3 gerandomiseerde gecontroleerde studie gepubliceerd in scalpel.
Omdat de studie, VLA1553-301, niet werd uitgevoerd in gebieden waar chikungunya endemisch is, konden de onderzoekers niet verifiëren of het vaccin beschermt tegen latere ziekten. In plaats daarvan testte de studie een immuunrespons op niveaus waarvan werd gedacht dat ze bescherming boden tegen ziekten als ze met het virus waren geïnfecteerd.
Chikungunya is een door muggen overgedragen ziekte die wordt veroorzaakt door het Chikungunya-virus (CHIKV), dat endemisch is in sommige regio’s van Afrika, Azië en Amerika. Het veroorzaakt koorts bij patiënten ongeveer vier tot acht dagen nadat ze zijn gebeten door een geïnfecteerde mug. Symptomen zijn hoofdpijn, vermoeidheid, misselijkheid en ernstige spier- en gewrichtspijn. De gewrichtspijn is vaak slopend en duurt meestal een paar dagen, maar kan ook weken, maanden of zelfs jaren aanhouden. Ernstige ziekte en overlijden zijn zeldzaam, maar ouderen en pasgeborenen lopen het grootste risico. Momenteel zijn er geen goedgekeurde vaccins om de ziekte veroorzaakt door een CHIKV-infectie te voorkomen en zijn er geen effectieve antivirale behandelingen voor de ziekte.
Hoofdauteur van de studie, dr. Martina Schneider, directeur van de klinische strategie bij Valneva, zegt: “Dit is mogelijk het eerste vaccin tegen chikungunya dat beschikbaar is voor mensen die in endemische gebieden wonen, maar ook voor mensen die naar endemische of risicovolle gebieden reizen. Onze veelbelovende resultaten toonden een goede stabiliteit in “antilichaamniveaus na vaccinatie, wat belangrijk is omdat chikungunya-uitbraken plotseling kunnen terugkeren. Aangezien leeftijd een risicofactor is voor de ernst en dood van chikungunya, is de robuuste immuunrespons die wordt waargenomen bij met name ouderen deelnemers kunnen nuttig zijn.”
Studieauteur Catherine Dubichard, directeur van het Chikungunya-vaccinatieprogramma in Valneva, zegt: “Momenteel is er geen specifieke behandeling of vaccin beschikbaar tegen Chikungunya, een slopende ziekte waarvan de symptomen op lange termijn kunnen aanhouden. Bovendien wordt het momenteel beschouwd als een van de de meest voorkomende virussen die zich mogelijk wereldwijd verspreiden, en studies hebben aangetoond dat klimaatverandering de oorzaak is van de verspreiding van muggen die het naar nieuwe delen van de wereld brengen, dus het hebben van een effectief vaccin is belangrijk om je voor te bereiden op toekomstige uitbraken.
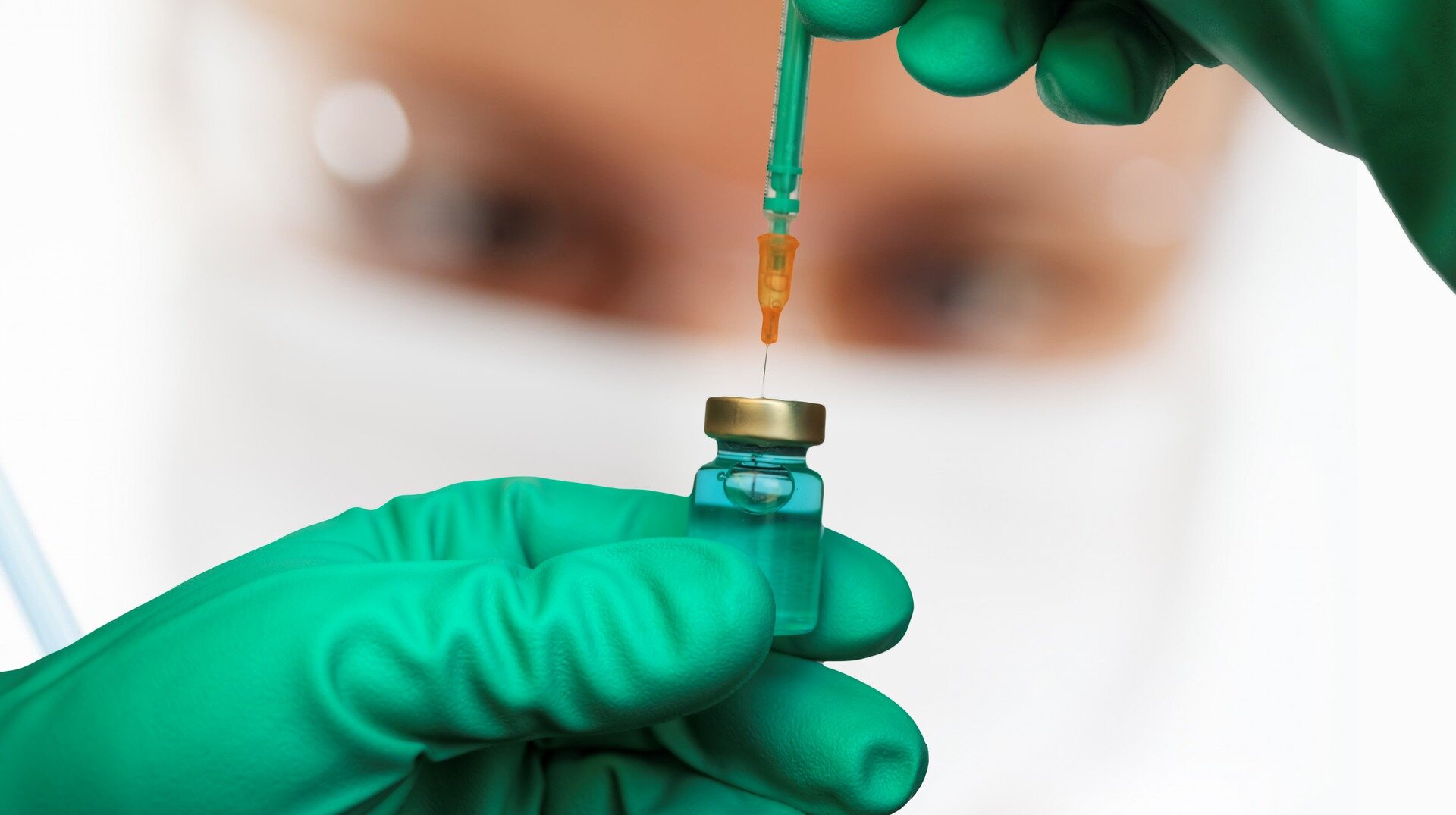
De studie omvatte 4.115 gezonde volwassenen op 43 onderzoekslocaties in de Verenigde Staten. Hiervan kregen 3082 deelnemers een enkele dosis VLA1553 (via een injectiespuit in de arm) en kregen 1033 deelnemers een placebo. Alle deelnemers werden opgenomen in de veiligheidsanalyse, maar de immuunrespons werd alleen getest in een subgroep van 362 deelnemers (266 kregen het vaccin en 96 kregen een placebo). De immuunresponsen van de deelnemers werden één week, 28 dagen, drie maanden en zes maanden na vaccinatie beoordeeld. Ze registreerden ook bijwerkingen in een elektronisch dagboek gedurende 11 dagen na vaccinatie. Degenen die binnen 21 dagen na vaccinatie bijwerkingen ondervonden (zoals koorts, gewrichtspijn, rugpijn, neurologische symptomen, hartproblemen, huiduitslag of zwelling) werden nauwlettend gevolgd.
Na een enkele vaccinatie induceerde VLA1553 antilichaamniveaus op een niveau dat beschermde tegen ziekte bij 99% (263/266) van de deelnemers. Er was geen verschil in de immuunrespons naar leeftijd.
VLA1553 werd over het algemeen goed verdragen door alle leeftijdsgroepen en de meeste bijwerkingen waren mild of matig. Bij degenen die het vaccin kregen, waren de meest voorkomende bijwerkingen hoofdpijn (ervaren door 32% van de gevaccineerde deelnemers), vermoeidheid (29%), spierpijn (24%), gewrichtspijn (18%) en pijn op de injectieplaats (13%). ).
Na zes maanden werden meer bijwerkingen geregistreerd bij degenen die met VLA1553 werden behandeld dan bij degenen die met een placebo werden behandeld. In totaal ondervond 51% (1.575/3.082) van de deelnemers die VLA1553 kregen en 31% (322/1033) van degenen die placebo kregen ten minste één bijwerking die als vaccinatiegerelateerd werd beschouwd. Het veiligheidsprofiel bij ouderen was vergelijkbaar met het veiligheidsprofiel bij volwassenen.
Ernstige bijwerkingen werden gemeld bij 2% (46/3.082) van de deelnemers die waren blootgesteld aan VLA1553 en bij 1% van de deelnemers in de placebo-arm (8/1.033). Twee daarvan zijn geclassificeerd als vaccingerelateerd. Een daarvan was een geval van milde myalgie bij een vrouw met een medische voorgeschiedenis van fibromyalgie, en het andere was een geval van koorts dat leidde tot ziekenhuisopname. Geen van deze gevallen resulteerde in de dood.
Het aantal miskramen dat werd waargenomen in de populatie die VLA1553 kreeg, was iets hoger dan verwacht in de algemene populatie (23% versus ongeveer 11-16%). Dit kan echter te wijten zijn aan natuurlijke variatie in de kleine steekproefomvang. Twee van de drie miskramen bij de vrouwen die VLA1553 kregen, werden verklaard door een genetische afwijking of een voorgeschiedenis van miskramen bij de deelnemers. In het resterende geval kan geen oorzaak worden vastgesteld en de auteurs merken op dat verdere monitoring nodig zal zijn naarmate het kandidaat-vaccin wordt gepubliceerd.
Dr. Juan Carlos Jaramillo, Chief Medical Officer van Valneva, gaf commentaar op de veiligheidsbevindingen van de studie: “De onafhankelijke Data Safety Monitoring Board (DSMB) evalueerde de veiligheidsgegevens tijdens de studie en stelde geen veiligheidsproblemen vast na evaluatie van alle gerapporteerde bijwerkingen. Twee ernstige bijwerkingen die tijdens de studie werden gemeld, herstelden volledig en werden beoordeeld door de DSMB, die geen zorgen uitte of van mening was dat er ernstige risico’s verbonden zijn aan vaccinatie in het algemeen.”
De auteurs wijzen op enkele beperkingen van hun studie. De studie werd niet uitgevoerd in een endemisch gebied, dus de reeds bestaande immuniteit van de deelnemers tegen het chikungunya-virus is onbekend, evenals de veiligheid van het vaccin in deze populatie. Bovendien is het vaccin gemaakt van een verzwakte versie van het levende virus, dus het is waarschijnlijk niet geschikt voor mensen met een verzwakt immuunsysteem en zwangere vrouwen. Ze erkennen ook dat, wil het chikungunya-vaccin zeer effectief zijn bij het beheersen van endemische ziekten, het ook aan kinderen moet worden gegeven. Om de veiligheid en werkzaamheid in deze leeftijdsgroep te bepalen, is er momenteel een onderzoek gaande bij adolescenten in endemische gebieden van Brazilië.
Dr. Katherine Stephenson, Centrum voor Virus- en Vaccinonderzoek van het Beth Israel Deaconess Medical Center, die niet betrokken was bij de studie, zei in een gerelateerde opmerking: “…de positieve resultaten van deze studie zijn zeer goed nieuws voor de paraatheid bij de CHIKV-pandemie CHIKV en andere virusinfecties blijven arbovirussen die wereldwijde bedreigingen vormen, gedreven door de uitbreiding van muggenhabitats als gevolg van klimaatverandering en de globalisering van handel en reizen. Verdere studies van VLA1553 in endemische gebieden en groeiende populaties, zoals de lopende proef bij adolescenten Brazilië (NCT04650399), zal van cruciaal belang zijn om de waarde van VLA1553 voor CHIKV-preventie te bevestigen, aangezien de real-world werkzaamheidsstudies zullen plaatsvinden in de context van een daadwerkelijke CHIKV-uitbraak.
meer informatie:
Veiligheid en immunogeniciteit van een enkelvoudig levend verzwakt chikungunya-vaccin: een dubbelblinde, multicenter, gerandomiseerde, placebogecontroleerde, fase 3-studie. scalpel (2023). www.thelancet.com/journals/lan… (23) 00641-4 / volledige tekst

“Gamedokter. Een zombiefanaat. Muziekstudio. Ninjacafé. Televisieliefhebber. Aardige fanatieke alcoholist.





More Stories
China is van plan het Tiangong-ruimtestation uit te breiden; Stel deze in op “Space Rule” omdat het ISS wordt uitgeschakeld
De Verenigde Staten detecteren het eerste geval van de H5N1-vogelgriep bij een varken, wat aanleiding geeft tot bezorgdheid voor de mens
NASA zal in 2025 de ruimtewandelingen aan boord van het internationale ruimtestation hervatten na een lek in het ruimtepak